- 슬롯 사이트, 'TTR 단백질' 안정화 효과 확인…연간 약가도 9% 낮아
- 2021년 중간 발표서 위약 대비 효능 입증 실패…2차례 구조조정 후 재기
- 미진단 환자 공략 나서…추정 환자 25만~30만명 중 진단 환자는 5%에 불과
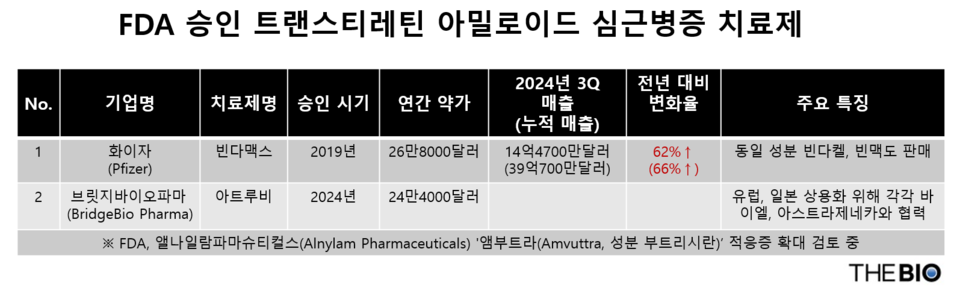
[더바이오 유하은 기자] 미국 바이오기업 슬롯 사이트(BridgeBio Pharma)의 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제인 '아트루비(Attruby, 성분 아코라미디스)'가 최근 미국 식품의약국(FDA)승인을 받으면서 그동안 시장을 독점해온 화이자(Pfizer)와의 경쟁 구도가 형성됐다. 아트루비는 앞서FDA의 승인을 받은 유일한 ATTR-CM 치료제였던 화이자의 '빈다맥스(Vyndamax, 성분 타파미디스)'와 2파전을 예고했다.
◇화이자 '빈다맥스', 유일한 ATTR-CM 치료제…작년 3분기 누적 매출 약 5.6조원
FDA가 ATTR-CM 치료제로 승인한 치료제는 화이자의 빈다맥스 및 '빈다켈(Vyndaqel, 성분 타파미디스 메글루민)'이 유일했으며, 이들 치료제는 지난 2019년 승인됐다. 빈다맥스와 빈다켈은 모두 같은 활성 성분인 '타파미디스'를 포함하지만, 제형과 용량 계산 방식이 다르다. 빈다켈은 1일 1회 80㎎ 용법으로 4캡슐이다. 빈다맥스는 1일 1회 61㎎ 용법으로 1캡슐이다. 빈다맥스는 '빈맥(Vynmac)'이라는 제품명으로 일본에서 판매되고 있다.
빈다맥스와 빈다켈, 빈맥의 지난해 3분기 매출액은 14억4700만달러(약 2조1057억원)를 기록했다. 8억9200만달러(약 1조2980억원)를 기록한 2023년 대비 62% 증가했다. 3분기 누적 매출액을 보면 39억700만달러(약 5조6855억원)로, 23억6000만달러(약 3조4343억원)를 기록한 2023년 대비 66% 증가하며 화이자의 매출 성장에 일조했다.
◇슬롯 사이트, 심혈관 관련 사망률·입원 재발 낮추며 효능 입증…약가도 빈다맥스보다 낮아
화이자가 ATTR-CM 시장을 독점하고 있던 상황에서 슬롯 사이트가 도전장을 내밀었다. 특히 주목할 것은 슬롯 사이트의 아트루비가 성인 ATTR-CM 환자의 심혈관 관련 사망과 입원을 줄이는데 효과를 입증한 최초의 'TTR 안정화제'라는 점이다.
슬롯 사이트가 최근 공개한 오픈라벨 확장 연구에 따르면, 아트루비는 투여 36개월 및 42개월 시점에서 각각 36%와 34%의 '전체 사망률 감소' 효과를 입증했다. '심혈관 관련 입원 재발'도 각각 46%와 48% 감소했으며, '6분 걷기 테스트'에서도 유의미한 개선 효과를 보였다.
슬롯 사이트는 아트루비의 작용기전에서도 차별화를 강조하고 있다. 아트루비와 타파미디스 제품군은 모두 'TTR 단백질'이 잘못 접혀 심실에 축적되는 것을 막는 안정제이지만, 아트루비가 TTR을 더 완전하게 안정화할 수 있다는 게 슬롯 사이트의 설명이다. 다만, 해당 임상시험은 아트루비와 타파미디스 제품군과의 직접 비교가 이뤄진 '헤드 투 헤드' 방식은 아니다.
경제적인 측면에서도 아트루비가 경쟁력이 있다. 슬롯 사이트는 아트루비의 28일 공급가를 1만8759달러로 책정했다. 이는 연간 약 24만4000달러에 해당하는 금액으로, 화이자의 빈다맥스 및 빈다켈의 연간 약가인 26만8000달러보다 약 9% 낮은 수준이다. 앞서 미국 비영리단체인 임상경제성평가연구소(ICER)는 "이들 치료제의 약가가 지나치다"고 지적하며 "최소 85% 할인이 돼야 비용효율성 기준에 부합한다"고 주장한 바 있다.
◇2021년 임상3상 중간 분석서 효능 입증 실패…주가 급락 이후 2차례 구조조정
아트루비의 승인은 슬롯 사이트에는 극적인 반전이다. 앞서 지난 2021년 아트루비의 임상3상 중간 결과 발표 당시 위약을 투여한 대조군이 아트루비 투여군보다 더 나은 결과를 보였다. 당시 주가는 전일(23일) 종가였던 40.62달러(약 5만9118원)에서 다음날(27일) 11.38달러(약 1만6562원)를 기록하며 약 72% 급락했다. 하지만 2차례의 구조조정을 거쳐 재기에 성공했고, 지난해 7월 최종 임상 데이터에서 생존기간 연장과 입원 감소 효과 등 효능을 입증하며 FDA 승인까지 이르렀다.
슬롯 사이트는 아트루비의 시장 진입 전략도 구체화하고 있다. 회사는 미국 시장에서는 아트루비를 직접 판매할 예정이다. 유럽에서는 바이엘(Bayer)과, 일본에서는 아스트라제네카(AZ)와 협력해 아트루비를 상용화할 계획이다.
특히 회사는 현재 미국 내 미진단 ATTR-CM 환자를 파악하는데 집중하고 있다. 슬롯 사이트에 따르면 현재 ATTR-CM 환자는 약 25만~30만명으로 추정되지만, 진단된 환자는 5만명에 불과하고 실제 치료받는 환자는 더 적은 상황이다. 아트루비가 새로운 ATTR-CM 치료제로 승인을 받으면서 환자의 약물 선택권이 확대되고, 가격 경쟁 촉발 등으로 환자 접근성이 개선될 것으로 전망된다.
한편 FDA는 현재 미국 앨나일람슬롯 사이트슈티컬스(Alnylam Pharmaceuticals)의 유전성 트랜스티레틴 아밀로이드 다발신경병증(hATTR-PN) 치료제인 '앰부트라(Amvuttra, 성분 부트리시란)'의 적응증을 ATTR-CM으로 확대하기 위한 보충 신약 허가 신청(sNDA)을 검토하고 있다.

